Chỉ định và Cách sử dụng Augmentin
Để giảm sự phát triển của vi khuẩn kháng thuốc và duy trì hiệu quả của Augmentin (amoxicillin / clavulanate kali) và các thuốc kháng khuẩn khác, chỉ nên sử dụng Augmentin để điều trị các bệnh nhiễm trùng đã được chứng minh hoặc nghi ngờ là do vi khuẩn nhạy cảm gây ra. Khi có thông tin về nuôi cấy và tính nhạy cảm, chúng nên được xem xét trong việc lựa chọn hoặc điều chỉnh liệu pháp kháng khuẩn. Trong trường hợp không có dữ liệu như vậy, dịch tễ học địa phương và các mô hình nhạy cảm có thể góp phần vào việc lựa chọn liệu pháp theo kinh nghiệm.
Augmentin ® là một chất kết hợp kháng khuẩn lớp penicilin và chất ức chế beta-lactamase được chỉ định trong điều trị nhiễm trùng do các chủng vi khuẩn được chỉ định nhạy cảm trong các điều kiện được liệt kê dưới đây *:
Nhiễm trùng đường hô hấp dưới
gây ra bởi các phân lập sản xuất beta ‑ lactamase của Haemophilus influenzae và Moraxella catarrhalis .
Phương tiện truyền thông viêm tai do vi khuẩn cấp tính
gây ra bởi các phân lập sản xuất beta-lactamase của H. influenzae và M. catarrhalis .
Viêm xoang
gây ra bởi các phân lập sản xuất beta-lactamase của H. influenzae và M. catarrhalis .
Nhiễm trùng da và cấu trúc da
gây ra bởi các phân lập sản xuất beta am lactamase của các loài Staphylococcus aureus, Escherichia coli và Klebsiella.
Nhiễm trùng đường tiết niệu
gây ra bởi các phân lập sản xuất beta ‑ lactamase của các loài E. coli, Klebsiella và các loài Enterobacter .
Hạn chế sử dụng
Khi kết quả kiểm tra độ nhạy cảm cho thấy nhạy cảm với amoxicillin, chứng tỏ không sản xuất beta-lactamase, không nên sử dụng Augmentin.
Liều lượng và cách dùng Augmentin
Augmentin có thể được thực hiện mà không liên quan đến bữa ăn; tuy nhiên, sự hấp thu của clavulanat kali được tăng cường khi dùng Augmentin vào đầu bữa ăn. Để giảm thiểu khả năng không dung nạp đường tiêu hóa, nên uống Augmentin vào đầu bữa ăn.
Người lớn
Liều thông thường cho người lớn là một viên Augmentin 500 mg mỗi 12 giờ hoặc một viên 250 mg Augmentin mỗi 8 giờ. Đối với các bệnh nhiễm trùng nặng hơn và nhiễm trùng đường hô hấp, liều dùng nên là một viên 875 mg Augmentin mỗi 12 giờ hoặc một viên Augmentin 500 mg mỗi 8 giờ. Người lớn gặp khó khăn khi nuốt có thể dùng hỗn dịch 125 mg / 5 mL hoặc 250 mg / 5 mL thay cho viên 500 mg. Hỗn dịch 200 mg / 5 mL hoặc hỗn dịch 400 mg / 5 mL có thể được sử dụng thay cho viên nén 875 mg.
Hai viên Augmentin 250 mg không được thay thế cho một viên Augmentin 500 mg. Vì cả viên nén 250 mg và 500 mg Augmentin đều chứa cùng một lượng axit clavulanic (125 mg, dưới dạng muối kali), hai viên nén 250 mg không tương đương với một viên 500 mg Augmentin.
Viên nén 250 mg Augmentin và viên nén 250 mg nhai không được thay thế cho nhau, vì chúng không thể thay thế cho nhau. Viên nén 250 mg Augmentin và viên nhai 250 mg không chứa cùng một lượng axit clavulanic (như muối kali). Viên nén 250 mg Augmentin chứa 125 mg axit clavulanic, trong khi viên nhai 250 mg chứa 62,5 mg axit clavulanic.
Bệnh nhân nhi
Dựa trên thành phần amoxicillin, Augmentin nên được định lượng như sau:
Trẻ sơ sinh và trẻ sơ sinh <12 tuần (<3 tháng) : Liều Augmentin được khuyến cáo là 30 mg / kg / ngày chia 12 giờ một lần, dựa trên thành phần amoxicillin. Kinh nghiệm với công thức 200 mg / 5 mL ở nhóm tuổi này còn hạn chế, do đó, khuyến cáo sử dụng hỗn dịch uống 125 mg / 5 mL.
Bệnh nhân từ 12 tuần tuổi (3 tháng) trở lên : Xem phác đồ dùng thuốc được cung cấp trong Bảng 1. Chế độ dùng thuốc 12 giờ một lần được khuyến cáo vì nó có liên quan đến tiêu chảy ít hơn đáng kể [xem Nghiên cứu lâm sàng (14.2)] . Tuy nhiên, hỗn dịch cứ sau 12 giờ (200 mg / 5 mL và 400 mg / 5 mL) và viên nén nhai (200 mg và 400 mg) có chứa aspartame và không được dùng bởi phenylketonurics. [xem Cảnh báo và Đề phòng (5.6) ]
Bảng 1: Liều lượng ở bệnh nhân từ 12 tuần tuổi (3 tháng) trở lên
| SỰ NHIỄM TRÙNG | ĐĂNG KÝ XỬ LÝ | |
| 12 giờ một lần | 8 giờ một lần | |
| 200 mg / 5 mL hoặc 400 mg / 5 mL hỗn dịch uống a | 125 mg / 5 mL hoặc 250 mg / 5 mL hỗn dịch uống a | |
| Viêm tai giữa b , viêm xoang, nhiễm trùng đường hô hấp dưới và các bệnh nhiễm trùng nặng hơn | 45 mg / kg / ngày mỗi 12 giờ | 40 mg / kg / ngày mỗi 8 giờ |
| Nhiễm trùng ít nghiêm trọng hơn | 25 mg / kg / ngày mỗi 12 giờ | 20 mg / kg / ngày mỗi 8 giờ |
a Mỗi độ mạnh của hỗn dịch Augmentin có sẵn dưới dạng viên nhai để trẻ lớn hơn sử dụng.
b Thời gian điều trị được nghiên cứu và khuyến cáo cho viêm tai giữa cấp tính là 10 ngày.
Bệnh nhân nặng từ 40 kg trở lên : Bệnh nhân nhi nặng từ 40 kg trở lên nên dùng liều theo khuyến nghị của người lớn.
Viên nén 250 mg Augmentin không nên được sử dụng cho đến khi trẻ nặng ít nhất 40 kg, do tỷ lệ amoxicillin và axit clavulanic khác nhau trong viên 250 mg Augmentin (250/125) so với viên nén 250 mg nhai của Augmentin (250 / 62,5).
Bệnh nhân suy thận
Bệnh nhân suy giảm chức năng thận thường không cần giảm liều trừ khi tình trạng suy giảm nghiêm trọng. Bệnh nhân suy thận có mức lọc cầu thận <30 mL / phút không nên dùng liều 875 mg. Bệnh nhân có mức lọc cầu thận từ 10 đến 30 mL / phút nên dùng 500 mg hoặc 250 mg mỗi 12 giờ, tùy thuộc vào mức độ nghiêm trọng của nhiễm trùng. Bệnh nhân có mức lọc cầu thận dưới 10 mL / phút nên được tiêm 500 mg hoặc 250 mg mỗi 24 giờ, tùy thuộc vào mức độ nghiêm trọng của nhiễm trùng.
Bệnh nhân thẩm tách máu nên nhận 500 mg hoặc 250 mg mỗi 24 giờ, tùy thuộc vào mức độ nghiêm trọng của nhiễm trùng. Họ sẽ nhận được một liều bổ sung cả trong và khi kết thúc lọc máu.
Hướng dẫn pha hỗn dịch uống
Chuẩn bị hỗn dịch tại thời điểm pha chế như sau: Nhấn vào chai cho đến khi tất cả bột chảy tự do. Thêm khoảng 2/3 tổng lượng nước để pha (xem Bảng 2 dưới đây) và lắc mạnh để bột huyền phù. Thêm phần nước còn lại và lắc mạnh một lần nữa.
Bảng 2: Lượng nước để pha hỗn dịch uống
| Sức mạnh | Kích thước chai | Lượng nước để tái tạo | Hàm lượng của mỗi Teaspoonful (5 mL) |
| 125 mg / 5 mL | 75 mL 100 mL 150 mL | 67 mL 90 mL134 mL | 125 mg amoxicilin và 31,25 mg axit clavulanic dưới dạng muối kali |
| 200 mg / 5 mL | 50 mL75 mL 100 mL | 50 mL75 mL95 mL | 200 mg amoxicillin và 28,5 mg axit clavulanic dưới dạng muối kali |
| 250 mg / 5 mL | 75 mL 100 mL 150 mL | 65 mL87 mL 130 mL | 250 mg amoxicillin và 62,5 mg axit clavulanic dưới dạng muối kali |
| 400 mg / 5 mL | 50 mL75 mL 100 mL | 50 mL 70 mL 90 mL | 400 mg amoxicillin và 57,0 mg axit clavulanic dưới dạng muối kali |
Lưu ý: Lắc kỹ hỗn dịch uống trước khi sử dụng. Hỗn dịch đã hoàn nguyên phải được bảo quản trong tủ lạnh và loại bỏ sau 10 ngày.
Dạng bào chế và độ mạnh
Máy tính bảng :
- Viên nén 250 – mg / 125 mg : Mỗi viên nén bao phim hình bầu dục màu trắng, được pha bằng Augmentin ở một mặt và 250/125 ở mặt còn lại, chứa 250 mg amoxicillin và 125 mg axit clavulanic dưới dạng muối kali.
- Viên nén 500 – mg / 125 mg : Mỗi viên nén bao phim hình bầu dục màu trắng, được pha bằng Augmentin ở một mặt và 500/125 ở mặt còn lại, chứa 500 mg amoxicillin và 125 mg axit clavulanic dưới dạng muối kali.
- Viên nén 875 – mg / 125 mg : Mỗi viên nén hình viên nang màu trắng được ghi điểm, được gắn Augmentin 875 ở một mặt và được ghi ở mặt còn lại, chứa 875 mg amoxicillin và 125 mg axit clavulanic dưới dạng muối kali.
Bột để đình chỉ uống:
- 125 mg / 31,25 mg mỗi 5 mL : Bột hương chuối để pha hỗn dịch uống (mỗi 5 mL hỗn dịch đã pha chứa 125 mg amoxicillin và 31,25 mg axit clavulanic dưới dạng muối kali).
- 200 mg / 28,5 mg mỗi 5 mL : Bột pha hỗn dịch uống có màu cam (mỗi 5 mL hỗn dịch đã pha chứa 200 mg amoxicillin và 28,5 mg axit clavulanic dưới dạng muối kali).
- 250 mg / 62,5 mg mỗi 5 mL : Bột hương cam pha hỗn dịch uống (mỗi 5 mL hỗn dịch đã pha chứa 250 mg amoxicillin và 62,5 mg axit clavulanic dưới dạng muối kali).
- 400 mg / 57 mg mỗi 5 mL Bột hương cam pha hỗn dịch uống (mỗi 5 mL hỗn dịch đã pha chứa 400 mg amoxicillin và 57,0 mg axit clavulanic dưới dạng muối kali).
Viên nén nhai được:
- Viên nén có thể nhai được 125 mg / 31,25-mg : Mỗi viên nén có màu vàng lốm đốm, hình tròn, có mùi chanh, được khử trùng với BMP 189 chứa 125 mg amoxicillin và 31,25 mg axit clavulanic dưới dạng muối kali.
- Viên nén có thể nhai 200 mg / 28,5 mg : Mỗi viên nén có màu hồng, hình tròn, hai mặt lồi có hương vị quả chuối-anh đào, được làm bằng Augmentin 200 chứa 200 mg amoxicillin và 28,5 mg axit clavulanic dưới dạng muối kali.
- Viên nén nhai được 250 mg / 62,5 mg : Mỗi viên nén có màu vàng lốm đốm, hình tròn, có mùi chanh, được tẩm bột BMP 190 chứa 250 mg amoxicillin và 62,5 mg axit clavulanic dưới dạng muối kali.
- Viên nén có thể nhai 400 mg / 57 mg : Mỗi viên nén có màu hồng, tròn, hai mặt lồi có hương vị chuối-anh đào, được làm với Augmentin 400 chứa 400 mg amoxicillin và 57,0 mg axit clavulanic dưới dạng muối kali.
Viên nén 250 mg Augmentin và viên nén 250 mg nhai KHÔNG được thay thế cho nhau, vì chúng không thể thay thế cho nhau và viên nén 250 mg không được dùng cho trẻ em cân nặng dưới 40 kg. Viên nén 250 mg Augmentin và viên nén 250 mg nhai không chứa cùng một lượng axit clavulanic. Viên nén 250 mg Augmentin chứa 125 mg axit clavulanic trong khi viên nén 250 mg nhai chứa 62,5 mg axit clavulanic.
Không nên thay thế hai viên 250 mg Augmentin cho một viên 500 mg Augmentin. Vì cả viên nén 250 mg và 500 mg Augmentin đều chứa cùng một lượng axit clavulanic (125 mg, dưới dạng muối kali), hai viên 250 mg Augmentin không tương đương với một viên Augmentin 500 mg.
Chống chỉ định
Phản ứng quá mẫn nghiêm trọng
Chống chỉ định dùng Augmentin ở những bệnh nhân có tiền sử phản ứng quá mẫn nghiêm trọng (ví dụ: phản vệ hoặc hội chứng Stevens-Johnson) với amoxicillin, clavulanate hoặc với các thuốc kháng khuẩn beta-lactam khác (ví dụ, penicillin và cephalosporin).
Vàng da ứ mật / Suy gan
Chống chỉ định dùng Augmentin ở những bệnh nhân có tiền sử vàng da ứ mật / rối loạn chức năng gan liên quan đến Augmentin.
Cảnh báo và đề phòng
Phản ứng quá mẫn
Các phản ứng quá mẫn (phản vệ) nghiêm trọng và đôi khi gây tử vong đã được báo cáo ở những bệnh nhân dùng kháng thể beta-lactam, bao gồm cả Augmentin. Những phản ứng này có nhiều khả năng xảy ra ở những người có tiền sử quá mẫn với penicillin và / hoặc tiền sử nhạy cảm với nhiều chất gây dị ứng. Trước khi bắt đầu điều trị với Augmentin, nên tìm hiểu kỹ về các phản ứng quá mẫn trước đó với penicilin, cephalosporin hoặc các chất gây dị ứng khác. Nếu phản ứng dị ứng xảy ra, nên ngừng sử dụng Augmentin và tiến hành liệu pháp thích hợp.
Rối loạn chức năng gan
Rối loạn chức năng gan, bao gồm viêm gan và vàng da ứ mật có liên quan đến việc sử dụng Augmentin. Nhiễm độc gan thường có thể hồi phục; tuy nhiên, các trường hợp tử vong đã được báo cáo. Nên theo dõi chức năng gan thường xuyên ở bệnh nhân suy gan.
Tiêu chảy liên quan đến Clostridium difficile (CDAD)
Tiêu chảy liên quan đến Clostridium difficile (CDAD) đã được báo cáo khi sử dụng gần như tất cả các chất kháng khuẩn, bao gồm cả Augmentin, và có thể có mức độ nghiêm trọng từ tiêu chảy nhẹ đến viêm đại tràng gây tử vong. Điều trị bằng các chất kháng khuẩn làm thay đổi hệ thực vật bình thường của ruột kết dẫn đến sự phát triển quá mức của C. difficile .
C. difficile tạo ra độc tố A và B góp phần vào sự phát triển của CDAD. Các chủng C. difficile sinh ra độc tố siêu vi khuẩn gây tăng tỷ lệ mắc bệnh và tử vong, vì những bệnh nhiễm trùng này có thể không điều trị bằng thuốc kháng sinh và có thể phải cắt bỏ. CDAD phải được xem xét ở tất cả những bệnh nhân bị tiêu chảy sau khi sử dụng thuốc kháng khuẩn. Cần cẩn thận tiền sử y tế vì CDAD đã được báo cáo là xảy ra hơn 2 tháng sau khi sử dụng các chất kháng khuẩn.
Nếu nghi ngờ hoặc xác nhận CDAD, việc sử dụng kháng khuẩn liên tục không hướng đến C. difficile có thể cần phải ngừng. Quản lý chất lỏng và điện giải thích hợp, bổ sung protein, điều trị kháng khuẩn C. difficile và đánh giá phẫu thuật nên được tiến hành theo chỉ định lâm sàng.
Phát ban da ở bệnh nhân tăng bạch cầu đơn nhân
Một tỷ lệ cao bệnh nhân bị tăng bạch cầu đơn nhân dùng amoxicillin bị phát ban đỏ trên da. Do đó, không nên dùng Augmentin cho bệnh nhân tăng bạch cầu đơn nhân.
Tiềm năng cho sự phát triển quá mức của vi sinh vật
Khả năng bội nhiễm với các mầm bệnh do nấm hoặc vi khuẩn nên được xem xét trong khi điều trị. Nếu xảy ra bội nhiễm, nên ngừng dùng amoxicillin / clavulanate potassium và điều trị thích hợp.
Phenylketonurics
Viên nén nhai Augmentin và Bột Augmentin cho Dung dịch uống chứa aspartame có chứa phenylalanin. Mỗi viên nhai Augmentin 200 mg chứa 2,1 mg phenylalanin; mỗi viên nhai 400 mg chứa 4,2 mg phenylalanin; mỗi 5 mL hỗn dịch uống 200 mg / 5 mL hoặc 400 mg / 5 mL chứa 7 mg phenylalanin. Các công thức khác của Augmentin không chứa phenylalanin.
Sự phát triển của vi khuẩn kháng thuốc
Kê đơn Augmentin trong trường hợp không có vi khuẩn đã được chứng minh hoặc nghi ngờ nhiễm trùng mạnh không có khả năng mang lại lợi ích cho bệnh nhân và làm tăng nguy cơ phát triển vi khuẩn kháng thuốc.
Phản ứng trái ngược
Những điều sau được thảo luận chi tiết hơn trong các phần khác của nhãn:
- Phản ứng phản vệ [xem Cảnh báo và Thận trọng (5.1) ]
- Rối loạn chức năng gan [xem Cảnh báo và Thận trọng (5.2) ]
- CDAD [xem Cảnh báo và Đề phòng (5.3) ]
Trải nghiệm thử nghiệm lâm sàng
Bởi vì các thử nghiệm lâm sàng được tiến hành trong các điều kiện khác nhau, tỷ lệ phản ứng có hại quan sát được trong các thử nghiệm lâm sàng của một loại thuốc không thể so sánh trực tiếp với tỷ lệ trong các thử nghiệm lâm sàng của một loại thuốc khác và có thể không phản ánh tỷ lệ quan sát được trong thực tế.
Các phản ứng phụ thường gặp nhất được báo cáo là tiêu chảy / phân lỏng (9%), buồn nôn (3%), phát ban và mày đay (3%), nôn (1%) và viêm âm đạo (1%). Ít hơn 3% bệnh nhân ngừng điều trị vì các phản ứng phụ liên quan đến thuốc. Tỷ lệ chung của các phản ứng có hại, và đặc biệt là tiêu chảy, tăng lên khi dùng liều khuyến cáo cao hơn. Các phản ứng ngoại ý khác ít được báo cáo hơn (<1%) bao gồm: Khó chịu ở bụng, đầy hơi và đau đầu.
Ở bệnh nhi (từ 2 tháng đến 12 tuổi), 1 thử nghiệm lâm sàng tại Hoa Kỳ / Canada đã được tiến hành so sánh 45 / 6,4 mg / kg / ngày (chia đều 12 giờ) của Augmentin trong 10 ngày so với 40/10 mg / kg / ngày (chia 8 giờ một lần) Augmentin trong 10 ngày trong điều trị viêm tai giữa cấp tính. Tổng cộng 575 bệnh nhân đã được ghi danh, và chỉ những công thức đình chỉ được sử dụng trong thử nghiệm này. Nhìn chung, các phản ứng bất lợi đã thấy có thể so sánh với phản ứng đã nêu ở trên; tuy nhiên, có sự khác biệt về tỷ lệ tiêu chảy, phát ban trên da / mày đay và phát ban vùng quấn tã. [Xem Nghiên cứu lâm sàng (14.2) ]
Kinh nghiệm tiếp thị sau
Ngoài các phản ứng bất lợi được báo cáo từ các thử nghiệm lâm sàng, những điều sau đây đã được xác định trong quá trình sử dụng Augmentin sau khi đưa ra thị trường. Bởi vì chúng được báo cáo một cách tự nguyện từ một quần thể không xác định, không thể ước tính tần suất. Những sự kiện này đã được chọn để đưa vào do sự kết hợp của mức độ nghiêm trọng, tần suất báo cáo hoặc mối liên hệ nhân quả tiềm ẩn với Augmentin.
Tiêu hóa: Khó tiêu, viêm dạ dày, viêm miệng, viêm lưỡi, lưỡi đen “có lông”, nhiễm nấm Candida da niêm mạc, viêm ruột và viêm đại tràng xuất huyết / giả mạc. Khởi phát các triệu chứng viêm đại tràng màng giả có thể xảy ra trong hoặc sau khi điều trị kháng sinh. [xem Cảnh báo và Đề phòng (5.3) ]
Phản ứng quá mẫn: Ngứa, phù mạch, phản ứng giống như bệnh huyết thanh (nổi mề đay hoặc phát ban da kèm theo viêm khớp, đau khớp, đau cơ và thường xuyên sốt), ban đỏ đa dạng, hội chứng Stevens ‑ Johnson, chứng ngoại ban toàn thân cấp tính, viêm mạch quá mẫn và các trường hợp viêm da tróc vảy (bao gồm hoại tử biểu bì nhiễm độc) đã được báo cáo. [xem Cảnh báo và Đề phòng (5.1) ]
Gan: Rối loạn chức năng gan, bao gồm viêm gan và vàng da ứ mật, tăng transaminase huyết thanh (AST và / hoặc ALT), bilirubin huyết thanh và / hoặc phosphatase kiềm, đã được báo cáo với Augmentin. Nó đã được báo cáo phổ biến hơn ở người cao tuổi, nam giới hoặc ở những bệnh nhân điều trị kéo dài. Các phát hiện mô học trên sinh thiết gan bao gồm những thay đổi chủ yếu của tế bào gan ứ mật, tế bào gan, hoặc hỗn hợp. Sự khởi đầu của các dấu hiệu / triệu chứng của rối loạn chức năng gan có thể xảy ra trong hoặc vài tuần sau khi ngừng điều trị. Rối loạn chức năng gan, có thể nghiêm trọng, thường có thể hồi phục được. Các trường hợp tử vong đã được báo cáo. [xem Chống chỉ định (4.2), Cảnh báo và Thận trọng (5.2) ]
Thận: Viêm thận kẽ, đái máu và đái ra tinh thể đã được báo cáo. [xem Quá liều lượng (10) ]
Hệ thống huyết và bạch huyết: Thiếu máu, bao gồm thiếu máu tan máu, giảm tiểu cầu, ban xuất huyết giảm tiểu cầu, tăng bạch cầu ái toan, giảm bạch cầu và mất bạch cầu hạt đã được báo cáo. Những phản ứng này thường hồi phục khi ngừng điều trị và được cho là hiện tượng quá mẫn. Tăng tiểu cầu được ghi nhận ở ít hơn 1% bệnh nhân được điều trị bằng Augmentin. Đã có báo cáo về việc tăng thời gian prothrombin ở những bệnh nhân dùng đồng thời Augmentin và liệu pháp chống đông máu. [xem Tương tác thuốc (7.2) ]
Hệ thần kinh trung ương: Kích động, lo lắng, thay đổi hành vi, lú lẫn, co giật, chóng mặt, mất ngủ và tăng động có hồi phục đã được báo cáo.
Khác: Sự đổi màu răng (màu nâu, vàng hoặc xám) đã được báo cáo. Hầu hết các báo cáo xảy ra ở bệnh nhi. Hầu hết các trường hợp đều giảm hoặc loại bỏ sự đổi màu khi đánh răng hoặc làm sạch răng.
Tương tác thuốc
Probenecid
Probenecid làm giảm bài tiết amoxicilin ở ống thận nhưng không làm chậm bài tiết acid clavulanic qua thận. Sử dụng đồng thời với Augmentin có thể làm tăng và kéo dài nồng độ amoxicillin trong máu. Không khuyến cáo dùng đồng thời với probenecid.
Thuốc uống chống đông máu
Thời gian prothrombin kéo dài bất thường (tăng tỷ lệ chuẩn hóa quốc tế [INR]) đã được báo cáo ở những bệnh nhân dùng amoxicillin và thuốc chống đông máu đường uống. Cần theo dõi thích hợp khi kê đơn đồng thời thuốc chống đông máu với Augmentin. Có thể cần điều chỉnh liều lượng thuốc chống đông máu đường uống để duy trì mức độ chống đông máu mong muốn.
Allopurinol
Việc sử dụng đồng thời allopurinol và amoxicillin làm tăng tỷ lệ phát ban ở bệnh nhân dùng cả hai loại thuốc so với bệnh nhân chỉ dùng amoxicillin. Người ta không biết liệu chứng phát ban do amoxicillin gây ra là do allopurinol hay do tăng acid uric máu ở những bệnh nhân này.
Thuốc uống tránh thai
Augmentin có thể ảnh hưởng đến hệ vi khuẩn đường ruột, dẫn đến giảm tái hấp thu estrogen và giảm hiệu quả của thuốc tránh thai kết hợp estrogen / progesterone dạng uống.
Ảnh hưởng đến các thử nghiệm trong phòng thí nghiệm
Nồng độ amoxicillin trong nước tiểu cao có thể dẫn đến phản ứng dương tính giả khi xét nghiệm sự hiện diện của glucose trong nước tiểu bằng cách sử dụng CLINITEST ® , Benedict’s Solution hoặc Fehling’s Solution. Vì tác dụng này cũng có thể xảy ra với Augmentin, nên sử dụng các xét nghiệm glucose dựa trên phản ứng enzym glucose oxidase.
Sau khi dùng amoxicillin cho phụ nữ có thai, sự giảm thoáng qua nồng độ trong huyết tương của tổng số estriol liên hợp, estriol-glucuronide, estrone liên hợp và estradiol đã được ghi nhận.
SỬ DỤNG TRONG DÂN SỐ CỤ THỂ
Thai kỳ
Tác dụng gây quái thai : Mang thai Loại B. Các nghiên cứu về sinh sản được thực hiện trên chuột mang thai và chuột được cho dùng Augmentin (công thức tỷ lệ 2: 1 của amoxicillin: clavulanate) ở liều uống lên đến 1200 mg / kg / ngày cho thấy không có bằng chứng về tác hại cho thai nhi do Augmentin . Liều amoxicillin ở chuột cống và chuột nhắt (dựa trên diện tích bề mặt cơ thể) xấp xỉ 4 và 2 lần so với liều uống tối đa ở người trưởng thành được khuyến cáo (875 mg mỗi 12 giờ). Đối với clavulanate, bội số liều này xấp xỉ 9 và 4 lần so với liều uống tối đa cho người lớn được khuyến cáo (125 mg mỗi 8 giờ). Tuy nhiên, không có nghiên cứu đầy đủ và có kiểm soát ở phụ nữ mang thai. Vì các nghiên cứu về sinh sản trên động vật không phải lúc nào cũng dự đoán được phản ứng của con người, thuốc này chỉ nên được sử dụng trong thời kỳ mang thai khi thật cần thiết.
Chuyển dạ và sinh đẻ
Thuốc kháng sinh nhóm ampicillin uống được hấp thu kém trong khi chuyển dạ. Người ta không biết liệu việc sử dụng amoxicillin / clavulanate potassium cho người trong khi chuyển dạ hoặc sinh nở có tác dụng phụ tức thời hay chậm trễ trên thai nhi, kéo dài thời gian chuyển dạ hoặc làm tăng khả năng cần can thiệp sản khoa hay không.
Các bà mẹ cho con bú
Amoxicillin đã được chứng minh là bài tiết qua sữa mẹ. Sử dụng amoxicillin / clavulanate kali cho bà mẹ cho con bú có thể dẫn đến mẫn cảm ở trẻ sơ sinh. Cần thận trọng khi dùng amoxicillin / clavulanate potassium cho phụ nữ đang cho con bú.
Sử dụng cho trẻ em
Tính an toàn và hiệu quả của Augmentin Powder để Treo và Viên nén nhai được đã được thiết lập ở bệnh nhân nhi. Sử dụng Augmentin ở bệnh nhân trẻ em được hỗ trợ bởi bằng chứng từ các nghiên cứu về Viên nén Augmentin ở người lớn với dữ liệu bổ sung từ một nghiên cứu về Augmentin Bột pha hỗn dịch uống ở bệnh nhi từ 2 tháng đến 12 tuổi bị viêm tai giữa cấp tính. [xem Nghiên cứu lâm sàng (14.2 )]
Do chức năng thận chưa phát triển hoàn thiện ở trẻ sơ sinh và trẻ nhỏ, việc thải trừ amoxicillin có thể bị trì hoãn; Sự thải trừ clavulanate không thay đổi ở nhóm tuổi này. Liều dùng của Augmentin nên được thay đổi ở bệnh nhi <12 tuần (<3 tháng). [xem Liều lượng và Cách dùng (2.2 ) ]
Sử dụng lão khoa
Trong số 3.119 bệnh nhân trong một phân tích các nghiên cứu lâm sàng của Augmentin, 32% là ≥65 tuổi, và 14% ≥75 tuổi. Không có sự khác biệt tổng thể về tính an toàn hoặc hiệu quả được quan sát thấy giữa những đối tượng này và đối tượng trẻ hơn, và kinh nghiệm lâm sàng được báo cáo khác đã không xác định được sự khác biệt về phản ứng giữa bệnh nhân cao tuổi và bệnh nhân trẻ tuổi, nhưng không thể loại trừ độ nhạy cao hơn ở một số người lớn tuổi.
Thuốc này được biết là bài tiết đáng kể qua thận và nguy cơ phản ứng có hại với thuốc này có thể lớn hơn ở những bệnh nhân bị suy giảm chức năng thận. Bởi vì bệnh nhân cao tuổi có nhiều khả năng bị giảm chức năng thận, nên cẩn thận trong việc lựa chọn liều lượng và có thể hữu ích để theo dõi chức năng thận.
Liều lượng trong suy thận
Amoxicillin được thải trừ chủ yếu qua thận và điều chỉnh liều thường được yêu cầu ở bệnh nhân suy thận nặng (GFR <30 mL / phút). Xem phần Bệnh nhân suy thận (2.3) để biết các khuyến nghị cụ thể ở bệnh nhân suy thận.
Quá liều lượng
Trong trường hợp quá liều, ngưng thuốc, điều trị triệu chứng và thực hiện các biện pháp hỗ trợ theo yêu cầu. Một nghiên cứu tiền cứu trên 51 bệnh nhi tại một trung tâm chống độc cho thấy rằng dùng quá liều dưới 250 mg / kg amoxicillin không liên quan đến các triệu chứng lâm sàng đáng kể 1 .
Đã có báo cáo về viêm thận kẽ dẫn đến suy thận oliguric ở những bệnh nhân sau khi dùng quá liều amoxicillin / clavulanate potassium.
Đái ra tinh thể, trong một số trường hợp dẫn đến suy thận, cũng đã được báo cáo sau khi dùng quá liều amoxicillin / clavulanate kali ở bệnh nhân người lớn và trẻ em. Trong trường hợp dùng quá liều, nên duy trì uống đủ nước và bài niệu để giảm nguy cơ kết tinh amoxicillin / clavulanate kali niệu.
Suy thận dường như có thể hồi phục khi ngừng sử dụng thuốc. Nồng độ cao trong máu có thể xảy ra dễ dàng hơn ở những bệnh nhân bị suy giảm chức năng thận do giảm độ thanh thải của amoxicillin / clavulanate kali qua thận. Amoxicillin / clavulanate kali có thể bị loại bỏ khỏi tuần hoàn bằng thẩm tách máu . [xem Liều lượng và Cách dùng (2.3 )]
Mô tả Augmentin
Augmentin là một sự kết hợp kháng khuẩn đường uống bao gồm amoxicillin và chất ức chế beta-lactamase, clavulanate kali (muối kali của axit clavulanic).
Amoxicillin là một chất tương tự của ampicillin, có nguồn gốc từ nhân penicillin cơ bản, axit 6 ‑ aminopenicillanic. Công thức phân tử amoxicillin là C 16 H 19 N 3 O 5 S • 3H 2 O, và khối lượng phân tử là 419,46. Về mặt hóa học, amoxicilin là (2S, 5R, 6R) -6 – [(R) – (-) – 2-Amino-2- (p-hydroxyphenyl) axetamido] -3,3-đimetyl-7-oxo-4-thia -1-azabicyclo [3.2.0] heptan-2-cacboxylic axit trihydrat và có thể được biểu thị về mặt cấu trúc là:
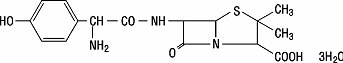
Axit clavulanic được tạo ra bằng cách lên men vi khuẩn Streptomyces clavuligerus . Nó là một beta-lactam có cấu trúc liên quan đến các penicilin và có khả năng vô hiệu hóa một số beta-lactamase bằng cách ngăn chặn các vị trí hoạt động của các enzym này. Công thức phân tử clavulanat kali là C 8 H 8 KNO 5 , và khối lượng phân tử là 237,25. Về mặt hóa học, clavulanat kali là kali (Z) (2R, 5R) -3- (2-hydroxyetyliden) -7-oxo-4-oxa-1-azabicyclo [3.2.0] -heptan-2-cacboxylat và có thể được biểu thị theo cấu trúc như:
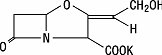
Thành phần không hoạt động:
- Máy tính bảng- Silicon dioxide dạng keo, hypromellose, magnesi stearat, cellulose vi tinh thể, polyethylene glycol, natri tinh bột glycolat, và titanium dioxide. Mỗi viên Augmentin chứa 0,63 mEq kali.
- Bột pha hỗn dịch uống, 125 mg / 5mL và 250 mg / 5mL – Silicon dioxide dạng keo, hương liệu, kẹo cao su xanthan, mannitol, axit succinic, silica gel và natri saccharin.
- Bột để treo, 200 mg / 5mL và 400 mg / 5mL – Silicon dioxide dạng keo, hương liệu, kẹo cao su xanthan, silica gel, hypromellose và aspartame [xem Cảnh báo và Thận trọng (5.6)]
- Viên nén nhai được, 125 mg và 250 mg – Silicon dioxide dạng keo, hương liệu, magie stearat, mannitol, natri saccharin, glycine và D&C Yellow No.10.
- Mỗi viên nhai 125 mg và mỗi 5 mL hỗn dịch uống 125/5 mL Augmentin đã hoàn nguyên chứa 0,16 mEq kali
- Mỗi viên nhai 250 mg và mỗi 5 mL hỗn dịch uống 250/5 mL Augmentin đã hoàn nguyên chứa 0,32 mEq kali
- Viên nén nhai được, 200 mg và 400 mg – Silicon dioxide dạng keo, hương liệu, magie stearat, mannitol, FD&C Red số 40 và aspartame. [xem Cảnh báo và Đề phòng (5.6)]
- Mỗi viên nhai 200 mg và mỗi 5 mL hỗn dịch uống 200/5 mL Augmentin đã hoàn nguyên chứa 0,14 mEq kali
- Mỗi viên nén nhai 400 mg và mỗi 5 mL hỗn dịch uống 400/5 mL Augmentin đã hoàn nguyên chứa 0,29 mEq kali
Augmentin – Dược lâm sàng
Cơ chế hoạt động
Augmentin là một loại thuốc kháng khuẩn. [xem Vi sinh 12.4 ]
Dược động học
Các thông số dược động học trung bình của amoxicillin và clavulanate kali ở người lớn bình thường sau khi sử dụng Viên nén Augmentin được trình bày trong Bảng 3 và sau khi sử dụng Augmentin Powder để treo và Viên nén nhai được trình bày trong Bảng 4.
Bảng 3: Trung bình (± SD) Amoxicillin và Clavulanate Kali Thông số dược động học a, b với Viên nén Augmentin
| Liều lượng và phác đồ | C tối đa (mcg / mL) | AUC 0-24 (mcg * h / mL) | ||
| Amoxicillin / Clavulanate kali | Amoxicillin | Clavulanat kali | Amoxicillin | Clavulanat kali |
| 250/125 mg mỗi 8 giờ | 3,3 ± 1,12 | 1,5 ± 0,70 | 26,7 ± 4,56 | 12,6 ± 3,25 |
| 500/125 mg mỗi 12 giờ | 6,5 ± 1,41 | 1,8 ± 0,61 | 33,4 ± 6,76 | 8,6 ± 1,95 |
| 500 125 mg cứ 8 giờ một lần | 7,2 ± 2,26 | 2,4 ± 0,83 | 53,4 ± 8,87 | 15,7 ± 3,86 |
| 875/125 mg mỗi 12 giờ | 11,6 ± 2,78 | 2,2 ± 0,99 | 53,5 ± 12,31 | 10,2 ± 3,04 |
Giá trị trung bình (± độ lệch chuẩn) của 14 người lớn bình thường (N = 15 đối với clavulanat kali trong chế độ liều thấp). Nồng độ đỉnh xảy ra khoảng 1,5 giờ sau khi dùng liều.
b Amoxicillin / clavulanate kali dùng khi bắt đầu bữa ăn nhẹ.
Bảng 4: Trung bình (± SD) Amoxicillin và Clavulanate Kali Thông số dược động học a, b với Bột Augmentin dùng để uống và viên nén nhai được
| Liều lượng | C tối đa (mcg / mL) | AUC 0-24 (mcg * h / mL) | ||
| Amoxicillin / Clavulanate kali | Amoxicillin | Clavulanat kali | Amoxicillin | Clavulanat kali |
| 400/57 mg (5 mL hỗn dịch) | 6,94 ± 1,24 | 1,10 ± 0,42 | 17,29 ± 2,28 | 2,34 ± 0,94 |
| 400/57 mg (1 viên nhai) | 6,67 ± 1,37 | 1,03 ± 0,33 | 17,24 ± 2,64 | 2,17 ± 0,73 |
a Giá trị trung bình (± độ lệch chuẩn) của 28 người trưởng thành bình thường. Nồng độ đỉnh xảy ra khoảng 1 giờ sau liều.
b Amoxicillin / clavulanate kali dùng khi bắt đầu bữa ăn nhẹ.
Uống 5 mL hỗn dịch 250 mg / 5 mL Augmentin hoặc liều tương đương 10 mL hỗn dịch 125 mg / 5 mL Augmentin cung cấp nồng độ đỉnh trung bình trong huyết thanh khoảng 1 giờ sau khi dùng 6,9 mcg / mL đối với amoxicilin và 1,6 mcg / mL đối với axit clavulanic. Diện tích dưới đường cong nồng độ huyết thanh thu được trong 4 giờ đầu tiên sau khi dùng thuốc là 12,6 mcg * h / mL đối với amoxicillin và 2,9 mcg * h / mL đối với axit clavulanic khi 5 mL hỗn dịch 250 mg / 5 mL Augmentin hoặc liều tương đương của 10 mL hỗn dịch 125 mg / 5 mL Augmentin được dùng cho người lớn bình thường. Một viên nén nhai 250 mg Augmentin hoặc hai viên nén nhai 125 mg Augmentin tương đương với 5 mL hỗn dịch 250 mg / 5 mL Augmentin và cung cấp nồng độ amoxicillin và axit clavulanic trong huyết thanh tương tự nhau.
Nồng độ amoxicilin trong huyết thanh đạt được với Augmentin tương tự như nồng độ được tạo ra khi uống với liều tương đương của một mình amoxicilin. Thời gian trên nồng độ ức chế tối thiểu 1 mcg / mL đối với amoxicillin đã được chứng minh là tương tự sau các chế độ dùng thuốc Augmentin cứ sau 12 giờ và 8 giờ tương ứng ở người lớn và trẻ em.
Hấp thu : Liều ở trạng thái lúc đói hoặc lúc ăn có ảnh hưởng tối thiểu đến dược động học của amoxicillin. Mặc dù Augmentin có thể được cung cấp mà không liên quan đến bữa ăn, sự hấp thụ của clavulanate kali khi uống cùng với thức ăn sẽ cao hơn so với trạng thái nhịn ăn. Trong một nghiên cứu, khả dụng sinh học tương đối của clavulanate bị giảm khi dùng Augmentin ở 30 phút và 150 phút sau khi bắt đầu bữa sáng nhiều chất béo.
Phân bố : Không thành phần nào trong Augmentin liên kết với protein cao; axit clavulanic liên kết khoảng 25% với huyết thanh người và amoxicillin liên kết khoảng 18%.
Amoxicillin dễ dàng khuếch tán vào hầu hết các mô và chất lỏng của cơ thể, ngoại trừ dịch não và tủy sống.
Hai giờ sau khi uống một liều duy nhất 35 mg / kg hỗn dịch Augmentin cho trẻ lúc đói, nồng độ trung bình 3 mcg / mL của amoxicilin và 0,5 mcg / mL axit clavulanic được phát hiện trong tràn dịch tai giữa.
Chuyển hóa và bài tiết: Thời gian bán hủy của amoxicillin sau khi uống Augmentin là 1,3 giờ và của axit clavulanic là 1 giờ.
Khoảng 50% đến 70% amoxicillin và khoảng 25% đến 40% axit clavulanic được bài tiết dưới dạng không đổi qua nước tiểu trong 6 giờ đầu sau khi dùng một viên Augmentin 250 mg hoặc 500 mg duy nhất.
Vi trùng học
Amoxicillin là một kháng sinh bán tổng hợp có hoạt tính diệt khuẩn in vitro chống lại vi khuẩn Gram dương và Gram âm. Tuy nhiên, amoxicillin dễ bị phân hủy bởi beta-lactamase, và do đó, phổ hoạt động không bao gồm các sinh vật tạo ra các enzym này. Axit clavulanic là một beta-lactam, có cấu trúc liên quan đến penicilin, có khả năng bất hoạt một số enzym beta-lactamase thường thấy ở vi sinh vật kháng penicilin và cephalosporin. Đặc biệt, nó có hoạt tính tốt chống lại các beta-lactamase qua trung gian plasmid quan trọng về mặt lâm sàng thường gây ra tình trạng kháng thuốc.
Công thức của amoxicillin và axit clavulanic trong Augmentin bảo vệ amoxicillin khỏi bị phân hủy bởi một số enzym beta-lactamase và mở rộng phổ kháng sinh của amoxicillin bao gồm nhiều vi khuẩn thường đề kháng với amoxicillin.
Amoxicillin / axit clavulanic đã được chứng minh là có hoạt tính chống lại hầu hết các chủng vi khuẩn sau đây, cả trong ống nghiệm và trong các trường hợp nhiễm trùng lâm sàng như được mô tả trong phần CHỈ ĐỊNH VÀ CÁCH DÙNG.
Vi khuẩn gram dương
Staphylococcus aureus
Vi khuẩn gram âm
Các loài Enterobacter
Escherichia coli
Haemophilus influenzae
Loài Klebsiella
Moraxella catarrhalis
Dữ liệu in vitro sau đây có sẵn, nhưng ý nghĩa lâm sàng của chúng vẫn chưa được biết . Ít nhất 90 phần trăm các vi khuẩn sau đây thể hiện nồng độ ức chế tối thiểu trong ống nghiệm (MIC) nhỏ hơn hoặc bằng điểm ngắt nhạy cảm đối với amoxicillin / axit clavulanic. Tuy nhiên, hiệu quả của amoxicillin / acid clavulanic trong điều trị nhiễm trùng lâm sàng do các vi khuẩn này chưa được thiết lập trong các thử nghiệm lâm sàng đầy đủ và có kiểm soát.
Vi khuẩn gram dương
Enterococcus faecalis
Staphylococcus epidermidis
Staphylococcus saprophyticus
Phế cầu khuẩn
Streptococcus pyogenes
Viridans nhóm Streptococcus
Vi khuẩn Gram âm
Eikenellacorrodens
Proteus mirabilis
Vi khuẩn k an khí
Bacteroidesspecies bao gồm Bacteroides fragilis
Các loài vi khuẩn Fusobacterium
Các loài peptostreptococcus
Phương pháp kiểm tra tính nhạy cảm
Khi có sẵn, phòng xét nghiệm vi sinh lâm sàng phải cung cấp kết quả xét nghiệm tính nhạy cảm in vitro đối với các sản phẩm thuốc kháng khuẩn được sử dụng trong bệnh viện nội trú cho bác sĩ dưới dạng báo cáo định kỳ mô tả hồ sơ tính nhạy cảm của các mầm bệnh mắc phải tại bệnh viện và cộng đồng. Các báo cáo này sẽ giúp bác sĩ lựa chọn một sản phẩm thuốc kháng khuẩn để điều trị.
Kỹ thuật pha loãng
Phương pháp định lượng được sử dụng để xác định nồng độ ức chế tối thiểu của kháng sinh (MIC). Các MIC này cung cấp các ước tính về tính nhạy cảm của vi khuẩn với các hợp chất kháng khuẩn. MIC phải được xác định bằng phương pháp thử tiêu chuẩn 2,3 (môi trường và / hoặc thạch). Các giá trị MIC phải được giải thích theo các tiêu chí được cung cấp trong Bảng 5.
Kỹ thuật khuếch tán :
Các phương pháp định lượng yêu cầu đo đường kính vùng cũng có thể cung cấp các ước tính có thể lặp lại được về tính nhạy cảm của vi khuẩn với các hợp chất kháng khuẩn. Kích thước vùng cung cấp ước tính về tính nhạy cảm của vi khuẩn đối với các hợp chất kháng khuẩn. Kích thước vùng cần được xác định bằng phương pháp thử tiêu chuẩn 3,4 . Quy trình này sử dụng đĩa giấy tẩm 30 mcg amoxicillin / axit clavulanic (20 mcg amoxicillin cộng với 10 mcg axit clavulanic) để kiểm tra tính nhạy cảm của vi khuẩn với amoxicillin / axit clavulanic. Các tiêu chí giải thích sự khuếch tán đĩa được cung cấp trong Bảng 5.
Bảng 5: Tiêu chí giải thích thử nghiệm tính nhạy cảm đối với Amoxicillin Acid Clavulanic
| Nồng độ ức chế tối thiểu (mcg / mL) | Khuếch tán đĩa (đường kính vùng tính bằng mm) | |||||
| Mầm bệnh | S | Tôi | R | S | Tôi | R |
| Enterobacteriaceae | 8/4 | 16/8 | 32/16 | > 18 | 14-17 | ≥13 |
| Haemophilus influenzae và Staphylococcus aureus | 4/2 | – | 8/4 | > 20 | – | ≤19 |
Kiểm soát chất lượng:
Các quy trình thử nghiệm tính nhạy cảm được tiêu chuẩn hóa yêu cầu sử dụng các biện pháp kiểm soát trong phòng thí nghiệm để theo dõi và đảm bảo độ chính xác và độ chính xác của vật tư và thuốc thử được sử dụng trong thử nghiệm cũng như các kỹ thuật của cá nhân thực hiện thử nghiệm 2,3,4 . Bột amoxicillin / axit clavulanic tiêu chuẩn phải cung cấp dải giá trị MIC sau được ghi chú trong Bảng 6 đối với kỹ thuật khuếch tán sử dụng 30 mcg amoxicillin / axit clavulanic (20 mcg amoxicillin cộng với 10 mcg axit clavulanic), các tiêu chí trong Bảng 6 cần đạt được .
Bảng 6: Phạm vi kiểm soát chất lượng được chấp nhận đối với Amoxicillin / Axit clavulanic
| QC Strain | Nồng độ ức chế tối thiểu (mcg / mL) | Khuếch tán đĩa (đường kính vùng tính bằng mm) |
| Escherichia coli ATCC 25922 | 2/1 đến 8/4 | 18 đến 24 |
| Escherichia coli ATCC 35218 | 4/2 đến 16/8 | 17 đến 22 |
| Haemophilus influenzae ATCC 49247 | 2/1 đến 16/8 | 15 đến 23 |
| Staphylococcus aureus ATCC 29213 | 0,12 / 0,06 đến 0,5 / 0,25 | – |
| Staphylococcus aureus ATCC 29523 | – | 28 đến 36 |
Độc chất học không lâm sàng
Sinh ung thư, Gây đột biến, Suy giảm khả năng sinh sản
Các nghiên cứu dài hạn trên động vật đã không được thực hiện để đánh giá khả năng gây ung thư.
Augmentin (công thức tỷ lệ 4: 1 của amoxicillin: clavulanate) không gây đột biến trong xét nghiệm đột biến vi khuẩn Ames và xét nghiệm chuyển đổi gen nấm men. Augmentin dương tính yếu trong xét nghiệm ung thư hạch ở chuột, nhưng xu hướng tăng tần số đột biến trong xét nghiệm này xảy ra ở liều lượng cũng liên quan đến giảm khả năng sống sót của tế bào. Augmentin âm tính trong thử nghiệm vi nhân trên chuột và trong thử nghiệm gây chết người chiếm ưu thế ở chuột. Riêng kali clavulanat đã được thử nghiệm trong xét nghiệm đột biến vi khuẩn Ames và trong xét nghiệm vi nhân trên chuột, và âm tính trong mỗi xét nghiệm này.
Augmentin (công thức tỷ lệ 2: 1 của amoxicillin: clavulanate) ở liều uống lên đến 1.200 mg / kg / ngày được phát hiện là không ảnh hưởng đến khả năng sinh sản và năng suất sinh sản ở chuột. Dựa trên diện tích bề mặt cơ thể, liều amoxicillin này gấp khoảng 4 lần liều uống tối đa cho người lớn được khuyến cáo (875 mg mỗi 12 giờ). Đối với clavulanate, bội số liều cao hơn khoảng 9 lần so với liều uống tối đa cho người lớn được khuyến cáo (125 mg mỗi 8 giờ), cũng dựa trên diện tích bề mặt cơ thể.
Các nghiên cứu lâm sàng
Đường hô hấp dưới và Nhiễm trùng đường tiết niệu phức tạp
Dữ liệu từ 2 thử nghiệm quan trọng trên 1.191 bệnh nhân được điều trị nhiễm trùng đường hô hấp dưới hoặc nhiễm trùng đường tiết niệu phức tạp so với phác đồ 875 mg viên nén Augmentin mỗi 12 giờ với viên nén Augmentin 500 mg mỗi 8 giờ (584 và 607 bệnh nhân, tương ứng). Hiệu quả so sánh đã được chứng minh giữa các chế độ dùng thuốc 12 giờ một lần và 8 giờ một lần. Không có sự khác biệt đáng kể về tỷ lệ các tác dụng phụ trong mỗi nhóm. Các tác dụng phụ thường được báo cáo là tiêu chảy; tỷ lệ mắc bệnh tương tự đối với các chế độ dùng thuốc 875 mg mỗi 12 giờ và 500 ‑ mg mỗi 8 giờ (tương ứng là 15% và 14%); tuy nhiên, có sự khác biệt có ý nghĩa thống kê (p <0,05) về tỷ lệ tiêu chảy nặng hoặc tiêu chảy rút lui giữa các phác đồ:
Trong một trong những thử nghiệm quan trọng này, bệnh nhân bị viêm thận bể thận (n = 361) hoặc nhiễm trùng đường tiết niệu phức tạp (tức là bệnh nhân có bất thường đường tiết niệu dẫn đến tái phát vi khuẩn niệu sau khi tiệt trừ, n = 268) được chọn ngẫu nhiên (1: 1) để nhận viên Augmentin 875 ‑ mg mỗi 12 giờ (n = 308) hoặc 500 ‑ mg viên Augmentin mỗi 8 giờ (n = 321).
Số lượng bệnh nhân được đánh giá về mặt vi khuẩn có thể so sánh giữa hai chế độ dùng thuốc. Augmentin tạo ra tỷ lệ vi khuẩn thành công tương đương ở những bệnh nhân được đánh giá từ 2 đến 4 ngày ngay sau khi kết thúc điều trị. Tỷ lệ hiệu quả vi khuẩn học có thể so sánh được ở một trong những lần tái khám (5 đến 9 ngày sau khi điều trị) và ở lần khám sau liệu pháp muộn (trong phần lớn các trường hợp, đây là 2 đến 4 tuần sau điều trị), như xem trong Bảng 7.
Bảng 7: Tỷ lệ hiệu quả vi khuẩn đối với Augmentin
| Thời gian trị liệu | 875 mg mỗi 12 giờ % (n) | 500 mg mỗi 8 giờ % (n) |
| 2 đến 4 ngày | 81% (58) | 80% (54) |
| 5 đến 9 ngày | 58% (41) | 52% (52) |
| 2 đến 4 tuần | 52% (101) | 55% (104) |
Như đã lưu ý trước đây, mặc dù không có sự khác biệt đáng kể về tỷ lệ các tác dụng ngoại ý ở mỗi nhóm, có sự khác biệt có ý nghĩa thống kê về tỷ lệ tiêu chảy nặng hoặc tiêu chảy rút lui giữa các phác đồ.
Viêm tai giữa do vi khuẩn cấp tính và tiêu chảy ở bệnh nhi
Một thử nghiệm lâm sàng tại Hoa Kỳ / Canada đã được thực hiện, so sánh 45 / 6,4 mg / kg / ngày (chia mỗi 12 giờ) của Augmentin trong 10 ngày so với 40/10 mg / kg / ngày (chia mỗi 8 giờ) của Augmentin trong 10 ngày trong điều trị viêm tai giữa cấp tính. Chỉ có các công thức đình chỉ được sử dụng trong thử nghiệm này. Tổng số 575 bệnh nhi (từ 2 tháng đến 12 tuổi) đã được thu nhận, với sự phân bổ đồng đều giữa 2 nhóm điều trị và số lượng bệnh nhân tương đương được đánh giá (tức là ³ 84%) cho mỗi nhóm điều trị. Các tiêu chí cụ thể của bệnh viêm tai giữa được yêu cầu để đủ điều kiện và mối tương quan chặt chẽ được tìm thấy khi kết thúc điều trị và theo dõi giữa các tiêu chí này và đánh giá của bác sĩ về đáp ứng lâm sàng. Tỷ lệ hiệu quả lâm sàng tại thời điểm kết thúc điều trị (được định nghĩa là 2‑4 ngày sau khi hoàn thành liệu pháp) và tại lần tái khám (được định nghĩa là 22‑28 ngày sau khi hoàn thành liệu pháp) là tương đương đối với 2 nhóm điều trị , với tỷ lệ chữa khỏi sau đây thu được cho những bệnh nhân được đánh giá: Khi kết thúc điều trị, 87% (n = 265) và 82% (n = 260) cho 45 mg / kg / ngày mỗi 12 giờ và 40 mg / kg / ngày mỗi 8 giờ, tương ứng. Tại thời điểm theo dõi, lần lượt là 67% (n = 249) và 69% (n = 243) đối với 45 mg / kg / ngày sau 12 giờ và 40 mg / kg / ngày sau 8 giờ.
Tiêu chảy được định nghĩa là: (a) 3 hoặc nhiều nước hoặc 4 hoặc nhiều hơn phân lỏng / nước trong 1 ngày; HOẶC (b) 2 lần phân lỏng mỗi ngày hoặc 3 lần phân lỏng / nhiều nước mỗi ngày trong 2 ngày liên tiếp. Tỷ lệ tiêu chảy thấp hơn đáng kể ở những bệnh nhân được điều trị theo chế độ 12 giờ một lần so với những bệnh nhân được sử dụng chế độ 8 giờ một lần (tương ứng là 14% và 34%). Ngoài ra, số lượng bệnh nhân bị tiêu chảy nặng hoặc đã hết tiêu chảy thấp hơn đáng kể ở nhóm điều trị 12 giờ một lần (3% và 8% cho mỗi 12 giờ / 10 ngày và 8 giờ / 10 ngày, tương ứng. ). Trong nhóm điều trị cứ sau 12 giờ, 3 bệnh nhân (1%) được rút thuốc do phản ứng dị ứng, trong khi 1 bệnh nhân trong nhóm cứ 8 giờ bị ngừng thuốc vì lý do này.
Người ta không biết liệu kết quả giảm tiêu chảy có ý nghĩa thống kê khi dùng hỗn dịch uống cứ 12 giờ một lần, so với hỗn dịch uống 8 giờ một lần, có thể được ngoại suy cho viên nén nhai hay không. Sự hiện diện của mannitol trong viên nhai có thể góp phần gây ra tình trạng tiêu chảy khác. Hỗn dịch uống cứ sau 12 giờ (200 mg / 5 mL và 400 mg / 5 mL) được làm ngọt bằng aspartame.
NGƯỜI GIỚI THIỆU
1. Swanson-Biearman B, Trưởng khoa BS, Lopez G, Krenzelok EP. Ảnh hưởng của việc uống penicilin và cephalosporin ở trẻ em dưới sáu tuổi. Năm 1988; 30: 66‑67.
2. Viện Tiêu chuẩn Lâm sàng và Phòng thí nghiệm (CLSI). Phương pháp pha loãng Thử nghiệm tính nhạy cảm với kháng sinh đối với vi khuẩn phát triển theo nhịp điệu; Tiêu chuẩn được phê duyệt – lần xuất bản thứ 8 . Tài liệu CLSI M7-A9. CLSI, 940 West Valley Road, Suite 1400, Wayne, PA, 19087, 2012.
3. Viện Tiêu chuẩn Phòng thí nghiệm và Lâm sàng (CLSI). Tiêu chuẩn hiệu suất cho các thử nghiệm tính nhạy cảm của đĩa kháng khuẩn; Tiêu chuẩn được phê duyệt – ấn bản lần thứ 11 . Tài liệu CLSI M2-A11. CLSI, 940 West Valley Road, Suite 1400, Wayne, PA, 19087, 2012.
4. GIẢI MÃ. Tiêu chuẩn thực hiện để kiểm tra tính nhạy cảm với kháng sinh: Bổ sung thông tin thứ 22 . Tài liệu CLSI M100-S22. CLSI, Wayne, PA, 2012.
Cách cung cấp / lưu trữ và xử lý
Máy tính bảng:
Viên nén 250 ‑ mg / 125 mg : Mỗi viên nén bao phim hình bầu dục màu trắng, được pha bằng Augmentin ở một mặt và 250/125 ở mặt còn lại, chứa 250mg amoxicillin dưới dạng trihydrat và 125mg axit clavulanic dưới dạng muối kali.
NDC 43598-018-30 chai 30
NDC 43598-018-78 Đơn vị Liều (10×10) 100 viên
Viên nén 500 ‑ mg / 125 mg : Mỗi viên nén bao phim hình bầu dục màu trắng, được trộn với Augmentin ở một mặt và 500/125 ở mặt còn lại, chứa 500mg amoxicillin dưới dạng trihydrat và 125mg axit clavulanic dưới dạng muối kali.
NDC 43598-006-14 chai 20
NDC 43598-006-78 Đơn vị Liều (10×10) 100 viên
Viên nén 875 ‑ mg / 125 mg : Mỗi viên nén hình viên nhộng màu trắng được ghi điểm, được gắn Augmentin 875 ở một mặt và được ghi ở mặt còn lại, chứa 875mg amoxicilin dưới dạng trihydrat và 125mg axit clavulanic dưới dạng muối kali.
NDC 43598-021-14 chai 20
NDC 43598-021-78 Liều lượng đơn vị (10×10) 100 viên
Bột pha hỗn dịch uống : 125 mg / 31,25 mg mỗi 5 mL : Bột hương chuối để pha hỗn dịch uống (mỗi 5 mL hỗn dịch hoàn nguyên chứa 125 mg amoxicillin và 31,25 mg axit clavulanic dưới dạng muối kali).
NDC 43598-012-51 chai 75 mL
NDC 43598-012-52 chai 100 mL
NDC 43598-012-53 chai 150 mL
200 mg / 28,5 mg mỗi 5 mL : Bột pha hỗn dịch uống có màu cam (mỗi 5 mL hỗn dịch đã pha chứa 200 mg amoxicillin và 28,5 mg axit clavulanic dưới dạng muối kali).
NDC 43598-013-50 chai 50 mL
NDC 43598-013-51 chai 75 mL
NDC 43598-013-52 chai 100 mL
250 mg / 62,5 mg mỗi 5 mL : Bột hương cam pha hỗn dịch uống (mỗi 5 mL hỗn dịch đã pha chứa 250 mg amoxicillin và 62,5 mg axit clavulanic dưới dạng muối kali).
NDC 43598-004-51 chai 75 mL
NDC 43598-004-52 chai 100 mL
NDC 43598-004-53 chai 150 mL
400 mg / 57 mg mỗi 5 mL Bột hương cam pha hỗn dịch uống (mỗi 5 mL hỗn dịch đã pha chứa 400 mg amoxicillin và 57,0 mg axit clavulanic dưới dạng muối kali).
NDC 43598-008-50 chai 50 mL
NDC 43598-008-51 chai 75 mL
NDC 43598-008-52 chai 100 mL
Viên nén nhai được : Viên nén nhai được 125-mg / 31,25-mg : Mỗi viên nén có màu vàng lốm đốm, hình tròn, có vị chanh, được làm bằng BMP 189, chứa 125 mg amoxicillin và 31,25 mg axit clavulanic dưới dạng muối kali.
NDC 43598-014-31 thùng 30 viên (5×6)
Viên nén nhai được 200 mg / 28,5 mg : Mỗi viên nén có màu hồng lốm đốm, hình tròn, hai mặt lồi, có hương vị chuối anh đào, được bổ sung Augmentin 200, chứa 200 mg amoxicillin và 28,5 mg axit clavulanic dưới dạng muối kali.
NDC 43598-015-14 thùng 20 viên
Viên nén nhai được 250 mg / 62,5-mg : Mỗi viên nén có màu vàng lốm đốm, hình tròn, có mùi chanh, được khử trùng với BMP 190, chứa 250 mg amoxicillin và 62,5 mg axit clavulanic dưới dạng muối kali.
NDC 43598-016-31 thùng 30 viên (5×6)
Viên nén có thể nhai 400 mg / 57 mg : Mỗi viên nén có màu hồng lốm đốm, hình tròn, hai mặt lồi, có mùi anh đào-chuối, được pha với Augmentin 400, chứa 400 mg amoxicillin và 57,0 mg axit clavulanic dưới dạng muối kali.
NDC 43598-017-14 thùng 20 viên
Phân phối trong thùng chứa ban đầu.
Bảo quản viên nén và bột khô ở hoặc dưới 25 ° C (77 ° F).
Bảo quản hỗn dịch đã pha trong tủ lạnh. Bỏ hỗn dịch không sử dụng sau 10 ngày.
Tránh xa tầm tay trẻ em.
Thông tin tư vấn cho bệnh nhân
Thông tin cho bệnh nhân
Bệnh nhân nên được thông báo rằng Augmentin có thể được dùng 8 giờ một lần hoặc 12 giờ một lần, tùy thuộc vào liều lượng được chỉ định. Mỗi liều nên được dùng trong bữa ăn chính hoặc bữa ăn nhẹ để giảm khả năng rối loạn tiêu hóa.
Bệnh nhân nên được tư vấn rằng thuốc kháng khuẩn, bao gồm cả Augmentin, chỉ nên được sử dụng để điều trị nhiễm trùng do vi khuẩn. Thuốc không điều trị nhiễm vi-rút (ví dụ, cảm lạnh thông thường). Khi Augmentin được kê đơn để điều trị nhiễm trùng do vi khuẩn, bệnh nhân nên được thông báo rằng mặc dù thông thường sẽ cảm thấy tốt hơn sớm trong quá trình điều trị, nhưng thuốc nên được dùng đúng theo chỉ dẫn. Bỏ qua liều hoặc không hoàn thành toàn bộ liệu trình có thể: (1) làm giảm hiệu quả của việc điều trị ngay lập tức và (2) tăng khả năng vi khuẩn phát triển kháng thuốc và sẽ không thể điều trị được bằng Augmentin hoặc các loại thuốc kháng khuẩn khác trong tương lai.
Tư vấn cho bệnh nhân rằng tiêu chảy là một vấn đề phổ biến do vi khuẩn gây ra và nó thường chấm dứt khi ngừng sử dụng kháng sinh. Đôi khi sau khi bắt đầu điều trị bằng kháng khuẩn, bệnh nhân có thể đi ngoài ra phân lỏng và có máu (kèm theo hoặc không kèm theo co thắt dạ dày và sốt), thậm chí muộn nhất là 2 tháng trở lên sau khi uống liều kháng khuẩn cuối cùng. Nếu tiêu chảy nặng hoặc kéo dài hơn 2 hoặc 3 ngày, bệnh nhân nên liên hệ với bác sĩ.
Bệnh nhân nên giữ hỗn dịch trong tủ lạnh. Lắc kỹ trước khi sử dụng. Khi định lượng cho trẻ với hỗn dịch (lỏng) của Augmentin, hãy sử dụng thìa định lượng hoặc ống nhỏ thuốc. Đảm bảo rửa sạch thìa hoặc ống nhỏ giọt sau mỗi lần sử dụng. Chai huyền phù của Augmentin có thể chứa nhiều chất lỏng hơn yêu cầu. Làm theo hướng dẫn của bác sĩ về số lượng sử dụng và những ngày điều trị mà con bạn yêu cầu. Bỏ thuốc không dùng đến.
Bệnh nhân cần lưu ý rằng Augmentin chứa một sản phẩm thuốc nhóm penicillin có thể gây ra phản ứng dị ứng ở một số người.
Augmentin là nhãn hiệu đã đăng ký của GlaxoSmithKline và được cấp phép cho Dr. Reddy’s Laboratories Inc.
CLINITEST là nhãn hiệu đã đăng ký của Miles, Inc.
Được sản xuất. Bởi:
Tiến sĩ Reddy’s Laboratories Tennessee LLC,
Bristol, TN 37620
Phát hành: 02/2014
BẢNG HIỂN THỊ HIỆU TRƯỞNG
NDC 43598-012-51
Augmentin ®
125 mg / 5 mL
AMOXICILLIN / CLAVULANATE POTASSIUM
ĐỐI VỚI TẠM NGỪNG ORAL
Khi hoàn nguyên, mỗi 5 mL chứa:
AMOXICILLIN, 125 MG,
như là trihydrate
AXIT CLAVULANIC, 31,25 MG,
như clavulanat kali
75 mL (khi hoàn nguyên)
R x chỉ
Hướng dẫn pha trộn:
Vòi chai cho đến khi tất cả bột chảy tự do. Thêm khoảng 2/3 tổng lượng nước để hoàn nguyên (tổng = 67 mL); lắc mạnh để bột ướt. Thêm nước còn lại; lại lắc mạnh.
Liều dùng : Xem thông tin kê đơn kèm theo.
Giữ chặt.
Lắc kỹ trước khi sử dụng.
Phải được bảo quản lạnh.
Bỏ sau 10 ngày.
Chỉ sử dụng nếu con dấu bên trong còn nguyên vẹn.
Hàm lượng thực : Tương đương với 1,875 g amoxicilin và 0,469 g axit clavulanic.
Bảo quản bột khô ở nhiệt độ phòng.
Được sản xuất. Bởi: Tiến sĩ Reddy’s Laboratories Tennessee LLC.
Bristol, TN 37620
I0414
150055049

BẢNG HIỂN THỊ HIỆU TRƯỞNG
NDC 43598-018-30
Augmentin ®
AMOXICILLIN / CLAVULANATE POTASSIUM BẢNG
AMOXICILLIN, 250 MG, ở dạng trihydrat
AXIT CLAVULANIC, 125 MG, dưới dạng clavulanat kali
30 viên nén
R x chỉ
Bảo quản ở nhiệt độ phòng. Phân phối trong thùng chứa ban đầu; khuyên bệnh nhân nên giữ trong bao bì kín. Mỗi viên chứa 250 mg amoxicillin dưới dạng trihydrat, 125 mg axit clavulanic ở dạng clavulanat kali.
Liều dùng: Xem thông tin kê đơn kèm theo.
Chỉ sử dụng nếu con dấu bên trong còn nguyên vẹn.
Được sản xuất. Bởi: Tiến sĩ Reddy’s Laboratories Tennessee LLC.
Bristol, TN 37620
150055043
I0414

BẢNG HIỂN THỊ HIỆU TRƯỞNG
NDC 43598-006-14
Augmentin ®
AMOXICILLIN / CALVULANATE POTASSIUM BẢNG
AMOXICILLIN, 500 MG, ở dạng trihydrat
AXIT CLAVULANIC, 125 MG, dưới dạng clavulanat kali
20 viên nén
R x chỉ
Bảo quản ở nhiệt độ phòng hoặc thấp hơn 25 o C (77 o F). Phân phối trong thùng chứa ban đầu; khuyên bệnh nhân nên giữ trong bao bì kín. Mỗi viên chứa 500 mg amoxicillin dưới dạng trihydrat, 125 mg axit clavulanic ở dạng clavulanat kali.
Liều dùng: Một viên sau mỗi 12 giờ. Xem thông tin kê đơn.
Chỉ sử dụng nếu con dấu bên trong còn nguyên vẹn.
Được sản xuất. Bởi: Tiến sĩ Reddy’s Laboratories Tennessee LLC.
Bristol, TN 37620
150055047
I0414

BẢNG HIỂN THỊ HIỆU TRƯỞNG
NDC 43598-021-14
Augmentin ®
AMOXICILLIN / CALVULANATE POTASSIUM BẢNG
AMOXICILLIN, 875 MG, ở dạng trihydrat
AXIT CLAVULANIC, 125 MG, dưới dạng clavulanat kali
20 viên nén
R x chỉ
Bảo quản ở nhiệt độ phòng hoặc thấp hơn 25 o C (77 o F). Phân phối trong thùng chứa ban đầu; khuyên bệnh nhân nên giữ trong bao bì kín. Mỗi viên chứa 875 mg amoxicillin dưới dạng trihydrat, 125 mg axit clavulanic ở dạng clavulanat kali.
Liều dùng: Một viên sau mỗi 12 giờ. Xem thông tin kê đơn.
Chỉ sử dụng nếu con dấu bên trong còn nguyên vẹn.
Được sản xuất. Bởi: Tiến sĩ Reddy’s Laboratories Tennessee LLC.
Bristol, TN 37620
150055048
I0414

BẢNG HIỂN THỊ HIỆU TRƯỞNG
NDC 43598-004-51
Augmentin ®
250 mg / 5 mL
AMOXICILLIN / CLAVULANATE POTASSIUM
ĐỐI VỚI TẠM NGỪNG ORAL
Khi hoàn nguyên, mỗi 5 mL chứa:
AMOXICILLIN, 250 MG,
như là trihydrate
AXIT CLAVULANIC, 62,5 MG,
như clavulanat kali
75 mL (khi hoàn nguyên)
R x chỉ
Hướng dẫn pha trộn:
Vòi chai cho đến khi tất cả bột chảy tự do. Thêm khoảng 2/3 tổng lượng nước để hoàn nguyên (tổng = 65 mL); lắc mạnh để bột ướt. Thêm nước còn lại; lại lắc mạnh.
Liều dùng : Xem thông tin kê đơn kèm theo.
Giữ chặt.
Lắc kỹ trước khi sử dụng.
Phải được bảo quản lạnh.
Bỏ sau 10 ngày.
Chỉ sử dụng nếu con dấu bên trong còn nguyên vẹn.
Hàm lượng thực : Tương đương 3,75 g amoxicilin và 0,938 g axit clavulanic.
Bảo quản bột khô ở nhiệt độ phòng.
Được sản xuất. Bởi: Tiến sĩ Reddy’s Laboratories Tennessee LLC.
Bristol, TN 37620
I0414
150055044

| Augmentin amoxicilin và clavulanat kali dạng viên, bao phim |
| Thông tin sản phẩmLoại sản phẩmNHÃN HIỆU THUỐC GIẢM CÂNMã hàng (Nguồn)NDC: 43598-018Con đường lãnh đạoORALLịch trình DEA |
| Thành phần hoạt tính / Chất hoạt tínhTên thành phầnCơ sở của sức mạnhSức mạnhAMOXICILLIN (AMOXICILLIN ANHYDROUS)AMOXICILLIN ANHYDROUS250 mgCLAVULANATE POTASSIUM (AXIT CLAVULANIC)AXIT CLAVULANIC125 mg |
| Thành phần không hoạt độngTên thành phầnSức mạnhSILICON DIOXIDE HYPROMELLOSES CHẤT MAGIÊ STEARATE CELLULOSE, MICROCRYSTALLINE POLYETHYLENE GLYCOLS SODIUM STARCH GLYCOLATE LOẠI MỘT KHOAI TÂY TITANIUM DIOXIDE |
| Đặc tính sản phẩmMàu sắcTRẮNGGhi bànkhông có điểmHình dạngHÌNH TRÁI XOANKích thước18mmHương vịMã nhà inAugmentin, 250; 125;Chứa đựng |
| Bao bì#Mã hàngMô tả gói1NDC: 43598-018-78100 TABLET, PHIM LỚN TRONG 1 HỘP, ĐƠN VỊ2NDC: 43598-018-3030 TABLET, PHIM LỚN TRONG 1 CHAI |
| Thông tin quảng bá sản phẩmHạng mục Tiếp thịSố đơn đăng ký hoặc trích dẫn chuyên khảoNgày bắt đầu tiếp thịNgày kết thúc tiếp thịNDANDA05056422/10/1990 |
| Augmentin amoxicilin và clavulanat kali dạng viên, bao phim |
| Thông tin sản phẩmLoại sản phẩmNHÃN HIỆU THUỐC GIẢM CÂNMã hàng (Nguồn)NDC: 43598-006Con đường lãnh đạoORALLịch trình DEA |
| Thành phần hoạt tính / Chất hoạt tínhTên thành phầnCơ sở của sức mạnhSức mạnhAMOXICILLIN (AMOXICILLIN ANHYDROUS)AMOXICILLIN ANHYDROUS500 mgCLAVULANATE POTASSIUM (AXIT CLAVULANIC)AXIT CLAVULANIC125 |
| Thành phần không hoạt độngTên thành phầnSức mạnhSILICON DIOXIDE HYPROMELLOSES CHẤT MAGIÊ STEARATE CELLULOSE, MICROCRYSTALLINE POLYETHYLENE GLYCOLS SODIUM STARCH GLYCOLATE LOẠI MỘT KHOAI TÂY TITANIUM DIOXIDE |
| Đặc tính sản phẩmMàu sắcTRẮNGGhi bànkhông có điểmHình dạngHÌNH TRÁI XOANKích thước20mmHương vịMã nhà inAugmentin, 500; 125;Chứa đựng |
| Bao bì#Mã hàngMô tả gói1NDC: 43598-006-78100 TABLET, PHIM LỚN TRONG 1 HỘP, ĐƠN VỊ2NDC: 43598-006-1420 TABLET, PHIM LỚN TRONG 1 CHAI |
| Thông tin quảng bá sản phẩmHạng mục Tiếp thịSố đơn đăng ký hoặc trích dẫn chuyên khảoNgày bắt đầu tiếp thịNgày kết thúc tiếp thịNDANDA05056422/10/1990 |
| Augmentin amoxicilin và clavulanat kali dạng viên, bao phim |
| Thông tin sản phẩmLoại sản phẩmNHÃN HIỆU THUỐC GIẢM CÂNMã hàng (Nguồn)NDC: 43598-021Con đường lãnh đạoORALLịch trình DEA |
| Thành phần hoạt tính / Chất hoạt tínhTên thành phầnCơ sở của sức mạnhSức mạnhAMOXICILLIN (AMOXICILLIN ANHYDROUS)AMOXICILLIN ANHYDROUS875 mgCLAVULANATE POTASSIUM (AXIT CLAVULANIC)AXIT CLAVULANIC125 |
| Thành phần không hoạt độngTên thành phầnSức mạnhSILICON DIOXIDE HYPROMELLOSES CHẤT MAGIÊ STEARATE CELLULOSE, MICROCRYSTALLINE POLYETHYLENE GLYCOLS SODIUM STARCH GLYCOLATE LOẠI MỘT KHOAI TÂY TITANIUM DIOXIDE |
| Đặc tính sản phẩmMàu sắcTRẮNGGhi bàn2 miếngHình dạngFREEFORM (Hình dạng viên nang)Kích thước22mmHương vịMã nhà inAugmentin; 875Chứa đựng |
| Bao bì#Mã hàngMô tả gói1NDC: 43598-021-78100 TABLET, PHIM LỚN TRONG 1 HỘP, ĐƠN VỊ2NDC: 43598-021-1420 TABLET, PHIM LỚN TRONG 1 CHAI |
| Thông tin quảng bá sản phẩmHạng mục Tiếp thịSố đơn đăng ký hoặc trích dẫn chuyên khảoNgày bắt đầu tiếp thịNgày kết thúc tiếp thịNDANDA05072010/02/1996 |
| Augmentin amoxicillin và bột kali clavulanate, để đình chỉ |
| Thông tin sản phẩmLoại sản phẩmNHÃN HIỆU THUỐC GIẢM CÂNMã hàng (Nguồn)NDC: 43598-012Con đường lãnh đạoORALLịch trình DEA |
| Thành phần hoạt tính / Chất hoạt tínhTên thành phầnCơ sở của sức mạnhSức mạnhAMOXICILLIN (AMOXICILLIN ANHYDROUS)AMOXICILLIN ANHYDROUS125 mg trong 5 mLCLAVULANATE POTASSIUM (AXIT CLAVULANIC)AXIT CLAVULANIC31,25 mg trong 5 mL |
| Thành phần không hoạt độngTên thành phầnSức mạnhSILICON DIOXIDE XANTHAN GUM ASPARTAME HYPROMELLOSES MANNITOL SACCHARIN SODIUM |
| Đặc tính sản phẩmMàu sắc Ghi bàn Hình dạngKích thướcHương vịTRÁI CHUỐIMã nhà inChứa đựng |
| Bao bì#Mã hàngMô tả gói1NDC: 43598-012-5175 mL trong 1 CHAI2NDC: 43598-012-52100 mL trong 1 CHAI3NDC: 43598-012-53150 mL trong 1 CHAI |
| Thông tin quảng bá sản phẩmHạng mục Tiếp thịSố đơn đăng ký hoặc trích dẫn chuyên khảoNgày bắt đầu tiếp thịNgày kết thúc tiếp thịNDANDA05057522/10/1990 |
| Augmentin amoxicillin và bột kali clavulanate, để đình chỉ |
| Thông tin sản phẩmLoại sản phẩmNHÃN HIỆU THUỐC GIẢM CÂNMã hàng (Nguồn)NDC: 43598-004Con đường lãnh đạoORALLịch trình DEA |
| Thành phần hoạt tính / Chất hoạt tínhTên thành phầnCơ sở của sức mạnhSức mạnhAMOXICILLIN (AMOXICILLIN ANHYDROUS)AMOXICILLIN ANHYDROUS250 mg trong 5 mLPHÂN LOẠI CLAVULANATE (AXIT CLAVULANIC)AXIT CLAVULANIC62,5 mg trong 5 mL |
| Thành phần không hoạt độngTên thành phầnSức mạnhSILICON DIOXIDE XANTHAN GUM ASPARTAME HYPROMELLOSES MANNITOL SACCHARIN SODIUM |
| Đặc tính sản phẩmMàu sắc Ghi bàn Hình dạngKích thướcHương vịTRÁI CAMMã nhà inChứa đựng |
| Bao bì#Mã hàngMô tả gói1NDC: 43598-004-5175 mL trong 1 CHAI2NDC: 43598-004-52100 mL trong 1 CHAI3NDC: 43598-004-53150 mL trong 1 CHAI |
| Thông tin quảng bá sản phẩmHạng mục Tiếp thịSố đơn đăng ký hoặc trích dẫn chuyên khảoNgày bắt đầu tiếp thịNgày kết thúc tiếp thịNDANDA05057522/10/1990 |
| Labeler – Tiến sĩ Reddy’s Laboratories Inc (802315887) |
| Người đăng ký – Dr. Reddy’s Laboratories Inc DBA Dr. Reddy’s Laboratories Tennessee LLC (967940441) |
| Thành lập | |||
| Tên | Địa chỉ | ID / FEI | Hoạt động |
| Tiến sĩ Reddy’s Laboratories Inc DBA Tiến sĩ Reddy’s Laboratories Tennessee LLC | 967940441 | sản xuất (43598-012, 43598-004, 43598-021, 43598-006, 43598-018) |
| Thành lập | |||
| Tên | Địa chỉ | ID / FEI | Hoạt động |
| Beecham Pharmaceuticals (PTE) Limited | 595132580 | sản xuất api (43598-018, 43598-006, 43598-021, 43598-012, 43598-004), phân tích (43598-018, 43598-006, 43598-021, 43598-012, 43598-004) |
| Thành lập | |||
| Tên | Địa chỉ | ID / FEI | Hoạt động |
| SmithKline Beecham Limited | 214482031 | sản xuất api (43598-018, 43598-006, 43598-021, 43598-012, 43598-004), phân tích (43598-018, 43598-006, 43598-021, 43598-012, 43598-004) |
Tiến sĩ Reddy’s Laboratories Inc
